Ácidos nucleicos
 El descubrimiento, en 1869, de la sustancia que resultó ser ácido desoxirribonucleico (ADN) fue de Friedrich Miescher, joven médico suizo que trabajaba en el laboratorio de Felix Hoppe-Seyler, químico fisiólogo alemán. Miescher trató glóbulos blancos (contenidos en la pus de vendas quirúrgicas desechadas) con ácido clorhídrico para obtener núcleos para estudio.
El descubrimiento, en 1869, de la sustancia que resultó ser ácido desoxirribonucleico (ADN) fue de Friedrich Miescher, joven médico suizo que trabajaba en el laboratorio de Felix Hoppe-Seyler, químico fisiólogo alemán. Miescher trató glóbulos blancos (contenidos en la pus de vendas quirúrgicas desechadas) con ácido clorhídrico para obtener núcleos para estudio.
Miescher llamó “nucleína” al precipitado, porque provenía de núcleos. Después, cuando se vio que era fuertemente ácido, su nombre cambió a ácido nucleico. Aunque no lo supo, Miescher había descubierto el ADN. Poco después, Hoppe-Seyler aisló una sustancia parecida de las células de levadura. Hoy se sabe que esa sustancia es ácido ribonucleico (ARN). Tanto ADN como ARN son polímeros de nucleótidos, o polinucleótidos.
En 1944, Oswald Avery, Colin MacLeod y Maclyn McCarty demostraron que el ADN es la molécula que contiene la información genética. En esos días se conocía muy poco acerca de la estructura de esta importante molécula. Durante los pocos años siguientes se determinaron las estructuras de los nucleótidos.
| En 1953, James D. Watson y Francis H. C. Crick propusieron su modelo de la estructura de ADN de doble hebra. |
Ahora se sabe que un organismo vivo contiene un conjunto de instrucciones para cada paso necesario para formar una réplica de sí mismo. Esa información reside en el material genético o genoma del organismo. Los genomas de todas las células están formados por ADN. Algunos genomas virales están formados por ARN. Un genoma puede consistir en una sola molécula de ADN, como en muchas especies de bacterias
Los nucleótidos son los bloques de construcción de los ácidos nucleicos
Los ácidos nucleicos son polinucleótidos, o polímeros de nucleótidos.
los nucleótidos tienen tres componentes:
- un azúcar con cinco carbonos,
- uno o más grupos fosfato
- y un compuesto nitrogenado débilmente básico llamado base
Las bases que se encuentran en los nucleótidos son pirimidinas y purinas sustituidas. La pentosa suele ser ribosa (D-ribofuranosa) o 2-desoxirribosa (2-desoxi-D-ribofuranosa). Los N-glicósidos pirimidina o purina de estos azúcares se llaman nucleósidos. Los nucleótidos son los ésteres de fosfato de los nucleósidos; los nucleótidos comunes contienen uno a tres grupos fosforilo. Los nucleótidos que contienen ribosa se llaman ribonucleótidos, y los que contienen desoxirribosa se llaman desoxirribonucleótidos.
Los nucleótidos son los bloques de construcción de los ácidos nucleicos.
En busca de nuevos fármacos a partir de ácidos nucleicos modificados
| Polímero de Azida |
Un aspecto en el que se diferencian de los medicamentos basados en anticuerpos es que los basados en ácidos nucleicos se pueden sintetizar. Desarrollamos y distribuimos microesferas de polímeros de alto rendimiento NittoPhase para la síntesis de medicamentos basados en ácidos nucleicos (portadores esenciales para la síntesis en fase sólida), además de proporcionar servicios y fabricar para empresas farmacéuticas y biotecnológicas especializadas en el desarrollo innovador de la medicina basada en ácidos nucleicos. NITTO DENKO Avecia se centra en esta labor y se encuentra en lo más alto en lo que se refiere a la fabricación con garantías de medicamentos basados en ácidos nucleicos.
Algunos Antibióticos
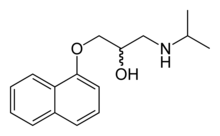
La Rifampicina es un antibiótico bactericida del grupo de las rifamicinas. Es un componente semisintético derivado deAmycolatopsis rifamycinica (previamente conocido como Amycolatopsis mediterranei y Streptomyces mediterranei). Dentro de la literatura la rifampicina puede ser abreviada como RIF, RMP, RD, RA o R.
La rifampicina inhibe la RNA polimerasa bacteriana mediante su unión a la subunidad beta de esta molécula.
Metronidazol
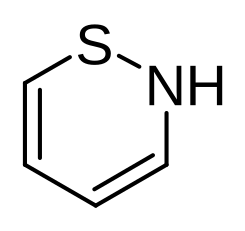
| estructura del Metronidazol |
Actinomicina
La actinomicina es el nombre aplicado a un grupo de antibióticos polipeptídicos aislados de las bacterias de suelo del género Streptomyces. Se utiliza principalmente como herramienta de investigación en biología celular para inhibir la transcripción. Esta inhibición la logra uniéndose al ADN en el complejo de iniciación de la transcripción y evitando así la elongación por la ARN polimerasa.
Quimioterapia
La actinomicina D se vende bajo el nombre comercial de Dactinomicina y es uno de los primeros fármacos utilizados durante muchos años en tratamientos de quimioterapia.
Se ofrece en forma de un líquido claro, de color amarillo, que se administra por vía intravenosa; es de uso común en el tratamiento de diversos tipos de cáncer, tales como:
- Neoplasia trofoblástica de la gestación (de alto riesgo)
- Tumor de Wilms
- Rabdomiosarcoma y otros sarcomas de partes blandas y ginecológicos
- Sarcoma de Ewing
Ribosa y desoxirribosa
Los azúcares componentes de los nucleótidos que se encuentran en los ácidos nucleicos. Los dos azúcares aparecen como proyecciones de Haworth de la configuración b de las formas de anillo de furanosa. Es la configuración estable que existe en los nucleótidos y polinucleótidos.
Purinas y pirimidinas
- Las bases que se encuentran en los nucleótidos son derivados de pirimidina o de purina
- La pirimidina tiene un solo anillo de cuatro átomos de carbono y dos de nitrógeno. La purina tiene un sistema de anillos fundidos de pirimidina y de imidazol. Los dos tipos de bases son no saturados, con dobles enlaces conjugados. Esta propiedad hace que los anillos sean planos, y también explica su capacidad de absorber la luz ultravioleta.
- La adenina, la guanina y la citosina están en ribonucleótidos y desoxirribonucleótidos. El uracilo se encuentra principalmente en ribonucleótidos y la timina en desoxirribonucleótidos.
- Las purinas y las pirimidinas son bases débiles relativamente insolubles en agua al pH fisiológico. Sin embargo, dentro de las células la mayor parte de bases pirimidina y purina se encuentran como constituyentes de nucleótidos y polinucleótidos, compuestos que son muy hidrosolubles.
Nucleósidos
- Los nucleósidos están formados por ribosa y desoxirribosa y una base heterocíclica. En cada nucleósido, un enlace b-N-glicosídico conecta el C-1 del azúcar al N-1 de la pirimidina o al N-9 de la purina.
- Los nombres de los nucleósidos se derivan de los de sus bases. El ribonucleósido que contiene adenina se llama adenosina (casi nunca se usa su nombre sistemático, 9-b-D-ribofuranosiladenina); su contraparte desoxi se llama desoxiadenosina. De igual modo, los ribonucleósidos de guanina, citosina y uracilo son guanosina, citidina y uridina, respectivamente.
Nucleótidos
Los nucleótidos son derivados fosforilados de los nucleósidos. Los ribonucleósidos contienen tres grupos hidroxilo que se pueden fosforilar (2 , 3 y 5 ), y los desoxirribonucleósidos contienen dos de esos grupos hidroxilo (3 y 5 ). En los nucleótidos naturales, los grupos fosforilo suelen estar unidos al átomo de oxígeno del grupo 5 -hidroxilo. Por convención, siempre se supone que un nucleótido es un éster de 5 -fosfato, a menos que se indique otra cosa,
- Los nombres sistemáticos de los nucleótidos indican la cantidad de grupos fosfato presentes. Por ejemplo, el éster 5 -monofosfato de la adenosina se llama adenosina monofosfato (AMP).
- Los nucleósidos monofosfato, que son derivados del ácido fosfórico, son aniónicos a pH fisiológico. Son ácidos dibásicos con valores de pKa aproximados entre 1 y 6. Los átomos de nitrógeno de los anillos heterocíclicos también se pueden ionizar.
El ADN tiene doble hebra
Hacia 1950 estaba claro que el ADN es un polímero lineal de residuos de 2 -desoxirribonucleótido unidos por 3 ,5 -fosfodiésteres. Erwin Chargaff había deducido ciertas regularidades en las composiciones de nucleótidos de muestras de ADN obtenidas de gran variedad de procariotas y eucariotas.
En general, los ADN de especies estrechamente relacionadas, como vacas, cerdos y humanos, tienen composiciones parecidas de bases. En el ADN de todas las especies, la relación de purinas a pirimidinas siempre es 1:1.
La tetraciclina es usada para tratar las infecciones provocadas por bacterias, incluyendo la neumonía y otras infecciones en las vías respiratorias; el acné; infecciones en la piel, los genitales y el sistema urinario; y la infección que causa úlceras estomacales (Helicobacter pylori). Este medicamento es también usado como una alternativa de otros medicamento para el tratamiento de la enfermedad de Lyme y para el tratamiento y prevención del carbunco (después de una exposición por inhalación). La tetraciclina pertenece a una clase de medicamentos llamados antibióticos de tetraciclina. Funciona al prevenir el crecimiento y diseminación de las bacterias. Los antibióticos no tienen ningún efecto en los resfríos, la gripe u otras infecciones víricas.
cloranfenicol, cloramfenicol

Antibiótico de amplio espectro que se emplea en el tratamiento contra las fiebres tifoideas.
Formación de una doble hélice con dos hebras anti paralelas
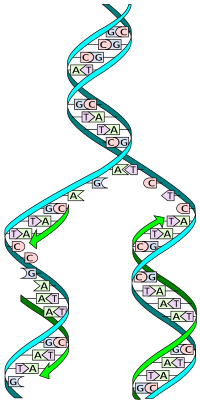 La mayor parte de las moléculas de ADN consisten de dos hebras, de polinucleótidos. Cada una de las bases en una hebra forma puentes de hidrógeno con una base de la hebra opuesta (figura 19.12). Los pares de bases más comunes están entre los tautómeros lactama y amino de las bases. La guanina se aparea con citosina y la adenina con timina, maximizando los puentes de hidrógeno entre sitios potenciales.
La mayor parte de las moléculas de ADN consisten de dos hebras, de polinucleótidos. Cada una de las bases en una hebra forma puentes de hidrógeno con una base de la hebra opuesta (figura 19.12). Los pares de bases más comunes están entre los tautómeros lactama y amino de las bases. La guanina se aparea con citosina y la adenina con timina, maximizando los puentes de hidrógeno entre sitios potenciales.
Entonces, los pares de bases G/C tienen tres puentes de hidrógeno, y los pares de bases A/T tienen dos. Esta propiedad del ADN de doble hebra explica el descubrimiento de Chargaff, de que la relación de A con T y de G con C es 1:1 para una gran variedad de moléculas de ADN. Como A en una hebra se aparea con T en la otra, y G se aparea con C, las hebras son complementarias, y una puede servir como plantilla para la otra.
Los esqueletos de azúcar-fosfato en las hebras complementarias de ADN de doble hebra tienen orientaciones opuestas.
En consecuencia, todas las moléculas de ADN tienen la misma estructura regular, a pesar de que puedan ser muy diferentes sus secuencias de nucleótidos.
- La doble hélice tiene dos surcos de ancho desigual, por la forma en que se apilan los pares de bases y en que se tuercen los esqueletos de azúcar-fosfato. Esos surcos se llaman surco mayor y surco menor (figura 19.14). Dentro de cada surco, los grupos funcionales en las orillas de los pares de bases quedan expuestos al agua. Cada par de bases tiene una pauta distintiva de grupos químicos en los surcos. Como los pares de bases son accesibles en los surcos, las moléculas que interactúan con determinados pares de bases pueden identificarlos sin alterar la hélice.
La longitud de las moléculas de ADN de doble hebra se expresa con frecuencia en términos de pares de bases (pb). Por comodidad, las estructuras más largas se miden en miles de pares de bases o kilopares de bases, que se abrevian kb.
Estabilización de la doble hélice por fuerzas débiles
1.Interacciones de apilamiento Los pares de bases apilados forman contactos de van der Waals. Aunque las fuerzas entre los pares de bases individuales apilados son débiles, son aditivas, por lo que en las moléculas grandes de ADN los contactos de van der Waals son una fuente importante de estabilidad.
2. Puentes de hidrógeno. Los puentes de hidrógeno entre pares de bases forman una importante fuerza estabilizadora.
3. Efectos hidrofóbicos. Al sepultar los anillos hidrofóbicos de purina y pirimidina en el interior de la doble hélice aumenta la estabilidad de la hélice.
4. Interacciones entre cargas. La repulsión electrostática de los grupos fosfato con carga negativa en el esqueleto es una fuente potencial de inestabilidad de la hélice de ADN. Sin embargo, la repulsión se minimiza por la presencia de cationes como y proteínas catiónicas (que contienen abundancia de los residuos básicos arginina y lisina).
Conformaciones de ADN de doble hebra
El ADN de doble hebra puede asumir distintas conformaciones bajo condiciones diferentes. Los estudios cristalográficos con rayos X de diversos oligodesoxirribonucleótidos sintéticos, de secuencia conocida, indican que las moléculas dentro de la célula no existen en una conformación B “pura”. En vez de ello, el ADN es una molécula dinámica cuya conformación exacta depende hasta cierto grado de las secuencia de nucleótidos. La conformación local también se afecta por dobleces en la molécula de ADN, y de si está unida a una proteína.
Superenrollamiento del ADN
Una molécula circular de ADN con la conformación B tiene un promedio de 10.4 pares de bases por vuelta. Se dice que está relajada si tal molécula puede reposar plana sobre una superficie. Esta doble hélice relajada se puede seguir envolviendo o desenvolviendo si se rompen las hebras del ADN y se tuercen los dos extremos de la molécula lineal en direcciones opuestas. Cuando se vuelven a unir las hebras para crear un círculo, ya no hay 10.4 pares de bases por vuelta, las necesarias para mantener la conformación B estable. La molécula circular se compensa por el envolvimiento o desenvolvimiento formando superenrollamientos que restauran 10.4 pares de bases por vuelta de la doble hélice (figura 19.19). Una molécula superenrollada de ADN no quedaría plana en una superficie. Cada superenrollamiento se compensa por una vuelta de la doble hélice.
Diversos tipos de ARN en las células
Las moléculas de ARN participan en varios procesos asociados a la expresión génica. Esas moléculas se encuentran en copias múltiples y en varias formas distintas dentro de una célula dada. Hay cuatro clases principales de ARN en todas las células vivas:
1. ARN ribosómico (ARNr); moléculas que son parte integral de los ribosomas (ribonucleoproteínas intracelulares que son sitios de síntesis de proteínas). El ARN ribosómico es la clase más abundante de ácido ribonucleico, que forma 80% del ARN celular total.
2. ARN de transferencia (ARNt); son moléculas que llevan a los aminoácidos activados a los ribosomas para su incorporación a las cadenas de péptidos en crecimiento durante la síntesis de proteínas. Las moléculas de ARNt sólo tienen de 73 a 95 residuos de nucleótidos de longitud. Forman un 15% del ARN celular total.
3. ARN mensajero(ARNm); moléculas que codifican las secuencias de aminoácidos en las proteínas. Son los “mensajeros” que llevan la información del ADN al complejo de traducción, donde se sintetizan las proteínas. En general, el ARNm sólo forma el 3% del ARN celular total. Estas moléculas son las menos estables de los ácidos ribonucleicos celulares.
4. ARN pequeño; moléculas presentes en todas las células. Algunas moléculas pequeñas de ARN tienen actividad catalítica o contribuyen a la actividad catalítica, asociadas a proteínas. Muchas de esas moléculas de ARN se relacionan con eventos de procesamiento que modifican al ARN después de que se ha sintetizado.
Los ARN son moléculas de una hebra, pero con frecuencia tienen estructura secundaria compleja. Bajo condiciones fisiológicas, la mayor parte de los polinucleótidos de una cadena se doblan hacia atrás sobre sí mismos para formar regiones estables de ARN de doble hebra, con bases apareadas
Empaquetamiento del ADN en cromatina, en células eucariotas
Nucleosomas
Las proteínas principales de la cromatina se llaman histonas. La mayoría de las especies eucarióticas tienen cinco histonas distintas, llamadas H1, H2A, H2B, H3 y H4. Las cinco histonas son proteínas pequeñas y básicas, que contienen numerosos residuos de lisina y arginina, cuyas cargas positivas permiten que las proteínas se unan al esqueleto de azúcar-fosfato, con carga negativa, del ADN.
La cromatina se desdobla al tratarla con una solución de poca fuerza iónica La fibra extendida de cromatina se ve como cuentas en un collar en una micrografía electrónica. Las “cuentas” son complejos de ADN-histonas llamados nucleosomas, y el “collar” es el ADN de doble cadena.
Niveles superiores de estructura de la cromatina
- El empaquetamiento de ADN en nucleosomas reduce aproximadamente a la décima parte la longitud de la molécula de ADN. Hay más reducción debida a mayores niveles de empacamiento del ADN. Por ejemplo, la estructura misma de cuentas en collar se enrolla y forma un solenoide, para llegar a la fibra de 30 nm.
- La fibra de 30 nm se forma cuando cada nucleosoma contiene una molécula de histona H1, y las moléculas adyacentes de H1 se unen entre sí, en forma cooperativa, acercando a los nucleosomas para crear una forma de cromatina más compacta y estable.
- La condensación de la estructura de “cuentas en collar” para formar un solenoide alcanza una reducción adicional a la cuarta parte de la longitud del cromosoma.
- mosoma.
- Por último, las fibras mismas de 30 nm se unen a un andamio de ARN-proteína que lleva a las fibras formando grandes bucles. Puede haber hasta 2 000 de esos bucles en un cromosoma grande.
A. Hidrólisis alcalina del ARN
La diferencia entre la ribosa del ARN y la 2 -desoxirribosa en el ADN puede parecer pequeña, pero afecta en gran medida las propiedades de los ácidos nucleicos. El grupo 2 -hidroxilo de la ribosa puede formar puentes de hidrógeno en algunas moléculas de ARN, y participa en ciertas reacciones químicas y catalizadas por enzimas.
B. Hidrólisis de ARN catalizada por ribonucleasa
La ribonucleasa pancreática bovina A (RNasa A) consiste en una sola cadena de polipéptido, de 124 residuos de aminoácidos con enlaces cruzados por cuatro puentes de disulfuro. La enzima tiene un pH óptimo aproximado de 6. La RNasa A cataliza la ruptura de enlaces de fosfodiéster en moléculas de ARN en los enlaces 5 -éster. En cadenas representadas en la dirección 5 → 3 , la escisión sucede a la derecha de los residuos de nucleótido de pirimidina.
C. Endonucleasas de restricción
Las endonucleasas de restricción son una subclase importante de endonucleasas que actúan sobre el ADN. El término endonucleasa de restricción se deriva de la observación que ciertas bacterias pueden bloquear infecciones de bacteriófagos (virus) destruyendo en forma específica al ADN del bacteriófago. Esas bacterias restringen la expresión de ADN extraño.
Se han caracterizado más de 200 endonucleasas de restricción deL tipo I y tipo II. En la tabla 19.4 se presentan las especificidades de algunas enzimas representativas. Casi en todos los casos, los sitios de reconocimiento tienen un eje de simetría doble; esto es, la secuencia 5 → 3 de residuos es igual en ambas hebras de la molécula de ADN.
D. Unión firme de EcoRI a ADN
Las endonucleasas de restricción se deben enlazar fuertemente al ADN para reconocer determinada secuencia y romper en determinado sitio. La estructura de EcoRI unida al ADN se ha determinado por cristalografía con rayos X. Como se ve en la figura 19.31, cada mitad del homodímero de EcoRI se une a un lado de la molécula de ADN,
Resumen de los vídeos
Replicación del ADN
- En primer lugar el ADN se desenrolla por la separación de puentes de Hidrógenos gracias a la enzima Helicasa, las proteínas enlazantes a cadena simple evitan que el ADN se enrolle de nuevo, lo cual crea una burbuja de replicacion por toda la molécula del ADN
- en una horquilla de la replicacion del ADN, el DNA polimerasa construye una nueva cadena
- necesita de algo para poder seguir, el ARN primasa, coloca los nucleotidos, entonces ARN cebador puede hacer que la Polimerasa pueda enlazarse y seguir construyendo.
- el ADN se sigue abriendo y desenrollándose, así la hebra crece cada vez mas, y se va replicando, luego otro DNA polimerasa remplaza el cebador.
- el ADN trae el Trisfosfato, la energía se usa la polimerizar la nueva cadena gracias a:
- la energía se libera
- el fosfato se une a un grupo OH libre
- se forman puentes de H entre nucleótidos
- Y así se polimeriza una nueva cadena de ADN
- Luego esta la hebra REZAGADA, se sintetiza en dirección opuesta, es la nueva hebra que crece en modo discontinuo, el ARN primasa, agrega el ARN cebador, entonces la DNA polimerasa sintetiza la nueva cadena, pero la hélice se va desenrollando de manera discontinua, y así sucesivamente.
- Los tramos discontinuos se llaman fragmentos de Okazaki
- un DNA polimerasa cambia el cebador ARN por ADN, este ADN polimerasa cambia así entonces el ARN por ADN
- Luego la Ligasa sella los tramos discontinuos, y así mientras la hélice se desenrolla
La nueva cadena es una copia exacta de la otra cadena parental, lo cual todo este proceso continua así hasta que ambas direcciones de la molécula completa de ADN haya sido replicada.
Hay múltiples burbujas por toda la molécula lo cual ayudaran a acelerar la velocidad, y continúan agrandándose hasta unirse y así tener dos nuevas moléculas de ADN.
Transcripción de ADN A ARN
- Este es el proceso mediante el ADN se copia a una nueva molécula, el ARN el cual empieza con lo que es el ensamblaje de un conjunto de factores en el inicio del gen.
- Entre esos factores el es ARN polimerasa, y otros mas se van ensamblando y de pronto este ARN es liberado por todo el ADN y leyendo el GEN pero a una velocidad muy rápida.
- A medida que el ARN polimerasa va desenrollando va copiando solo UNA de las dos hebras, lo cual va haciendo una copia idéntica, en el vídeo se muestra amarilla, lo cual allí lleva una copia del mensaje genético, ocurre así por toda la molécula del ADN.
- Los bloques de Nucleótidos se utilizan para hacer el nuevo ARN que lleva la información, entran entran a través de un túnel que tiene el ARN Polimerasa, lo cual en el centro activo, se aparean con el ADN copiando, las ACTG pero lo cual en la copia, osea el ARN, lo cual la T es reemplazada por U (Uracilo).
Traducción(de ADN a proteína)


- RNAm Eucariota 3´ a 5´
- Compuesta por una cola POLY-A, también contiene Codones que codifican Aminoácidos específicos.
- al final cual se encuentra una capa metilada.
El ribosoma esta compuesta por:
- Una unidad grande
- Una unidad pequeña
Contiene también un antidocon que es complementaria a donde se unirá, el primero es AUG.
La unidad pequeño posiciona al ARNm para que pueda ser leído en grupo de 3 a.a. conocidos como codones.
- La unidad grande remueve a los a.a., mientras que el ARNm pasa por el ribosoma es traducido a una secuencia de a.a. lo cual se encuentra en la punta del ARNt.
- La unidad grande se une para formar el sitio A y el P, el primer ARN se une al sitio A luego al P.
- Esto es complementario al segundo codon del ARNm.
El ribosoma se mueve a través del ARNm, y así sucesivamente, mientras que el peptidos creciente se trasladada al sitio A, y entra un nuevo ARNt, lo cual un codon de paro, un factor de liberación entra al sitio A y termina todo, lo cual la proteína recién creada es liberada.